
相關聯結
|
藥品資訊
 |
 |
 |
| |
藥品資訊內容
| 語音自動播報
|
|
Lenvima 10mg/Cap |
|
樂衛瑪膠囊 |
|
HD07M1 |
|
L01EX08 |
|
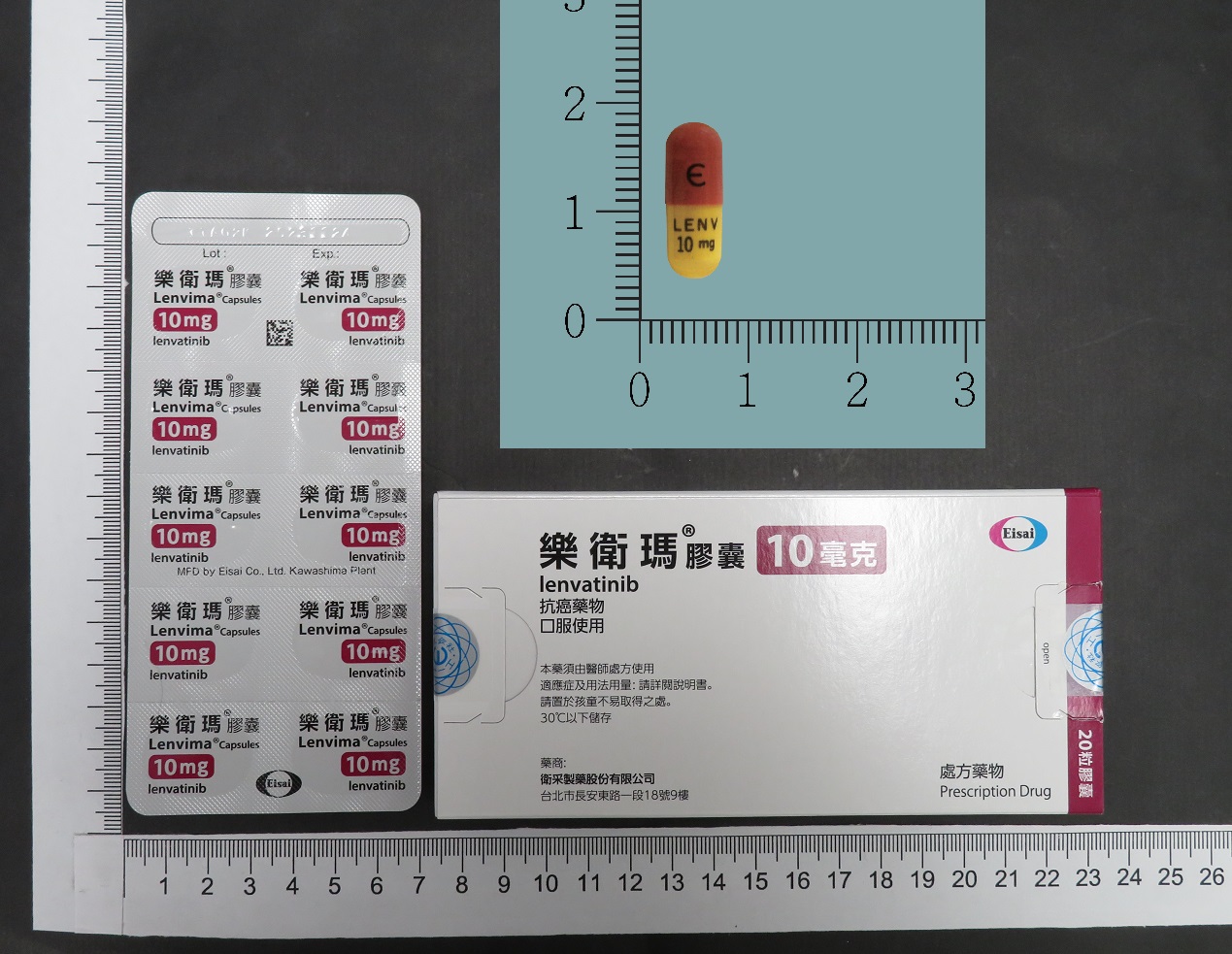 JPG下載
JPG下載
|
|
Lenvatinib mesilate |
|
10mg/Cap |
|
膠囊劑 |
|
Antineoplastic Agents |
|
|
|
衛采 |
|
|
|
BC26934100 |
|
衛部藥輸字第026934號 |
|
1. 分化型甲狀腺癌(Differentiated thyroid cancer, DTC): 適用於放射性碘治療無效之進行性,且為局部晚期或轉移性之分化型甲狀腺癌之成人病人。
2. 腎細胞癌(Renal Cell Carcinoma, RCC): 適用於和everolimus併用治療曾經接受過一種抗血管新生療法的晚期腎細胞癌病人。
3. 肝細胞癌(Hepatocellular Carcinoma): 適用於無法手術切除且不適合局部治療之晚期肝細胞癌病人。
4. 子宮內膜癌(Endometrial Carcinoma): 與pembrolizumab併用適用於曾經接受過全身性治療後疾病惡化,且不適合根治手術或放射治療的不具有高微衛星不穩定性(microsatellite instability-high, MSI-H)或錯誤配對修復功能不足(mismatch repair deficient, dMMR)之晚期子宮內膜癌病人。 |
|
Lenvatinib 是一種receptor tyrosine kinase (RTK) 抑制劑,會抑制血管內皮生長因子 (VEGF) 受體VEGFR1 (FLT1)、VEGFR2 (KDR) 和VEGFR3 (FLT4)之激酶活性。除了抑制一般細胞功能外,lenvatinib 還會抑制促病因性血管增生、腫瘤生長和癌症惡化相關之RTKs 活性,包括纖維母細胞生長因子 (FGF)受體FGFR1、2、3、4;血小板衍生生長因子受體 (PDGFRα)、KIT RET。
Lenvatinib 與everolimus 的併用能增強抗血管新生及抗腫瘤的效果,其效果在體外試驗中能減少人類內皮細胞的增生、血管生成及VEGF 的訊息傳遞,以及在小鼠異種移植研究模型中,合併使用比單獨使用更縮小人類腎細胞癌的腫瘤體積而得以證實。 |
|
依據作用機轉及動物生殖試驗數據,懷孕婦女使用Lenvima 會對胎兒造成傷害。 |
|
分化型甲狀腺癌 (DTC) 的建議劑量
Lenvima® 每日建議劑量為24mg,每日一次,隨餐或空腹口服使用。持續使用Lenvima® 直到疾病惡化或發生無法接受之毒性。
腎細胞癌 (RCC) 的建議劑量
Lenvima 每日建議劑量為18mg,併用5mg everolimus,每日一次,隨餐或空腹口服使用。
持續使用Lenvima 與everolimus 直到疾病惡化或發生無法接受之毒性。 |
|
高血壓、疲勞、腹瀉、關節痛/肌肉疼痛、食慾減退、體重減輕、噁心、口腔炎、頭痛、嘔吐、蛋白尿、肢端紅腫症 (PPE)、肺炎。 |
|
|
|
1. 膠囊應整粒吞服,或將膠囊先溶解於小杯液體後服用。吞嚥困難的病人,可量取一大湯匙的水或蘋果汁於玻璃杯中後放入膠囊 (膠囊不需打開或壓碎)。將膠囊靜置於液體中至少10分鐘,攪拌至少3分鐘後,飲用液體。飲用後,再加入等量(一大湯匙) 的水或蘋果汁於玻璃杯中,混勻後再飲用完剩餘的液體。
2. Lenvima 須於每日同一時間服用。如果忘記服藥並且未能在12小時內服用,應略過該次劑量並且於原定服藥時間投予下一次劑量。
3. 有生育能力的婦女於Lenvima治療期間直到完成治療後至少2週應採取有效之避孕措施。
4. 治療期間停止哺乳。 |
|
|
|
9.63.Lenvatinib(如Lenvima):(107/7/1、109/1/1、109/8/1)
1.用於放射性碘治療無效之局部晚期或轉移性的進行性(progressive)分化型甲狀腺癌(RAI-RDTC):
(1)需經事前審查核准後使用,每次申請之療程以3個月為限,送審時需檢送影像資料,每3個月評估一次。
(2)Lenvatinib與sorafenib不得合併使用。(109/8/1)
2.晚期肝細胞癌部分:(109/1/1、109/8/1)
(1)轉移性或無法手術切除且不適合局部治療或局部治療失敗之Child-Pugh A class晚期肝細胞癌成人患者,並符合下列條件之一:
I.肝外轉移(遠端轉移或肝外淋巴結侵犯)。
II.大血管侵犯(腫瘤侵犯主門靜脈或侵犯左/右靜脈第一或第二分支)。
III.經導管動脈化學藥物栓塞治療(Transcatheter arterial chemo embolization, T.A.C.E.)失敗者,需提供患者於12個月內>=3次局部治療之記錄。
(2)需經事前審查核准後使用,初次申請之療程以3個月為限,之後每2個月評估一次。送審時需檢送影像資料,無疾病惡化方可繼續使用。
(3)Lenvatinib與sorafenib僅得擇一使用,不得互換;且lenvatinib治療失敗後,不得申請使用Stivarga或Opdivo。(109/1/1、109/8/1) |
|
|
|
|
|
|
 |
 |
 |
|