藥品資訊內容
| 語音自動播報
|
|
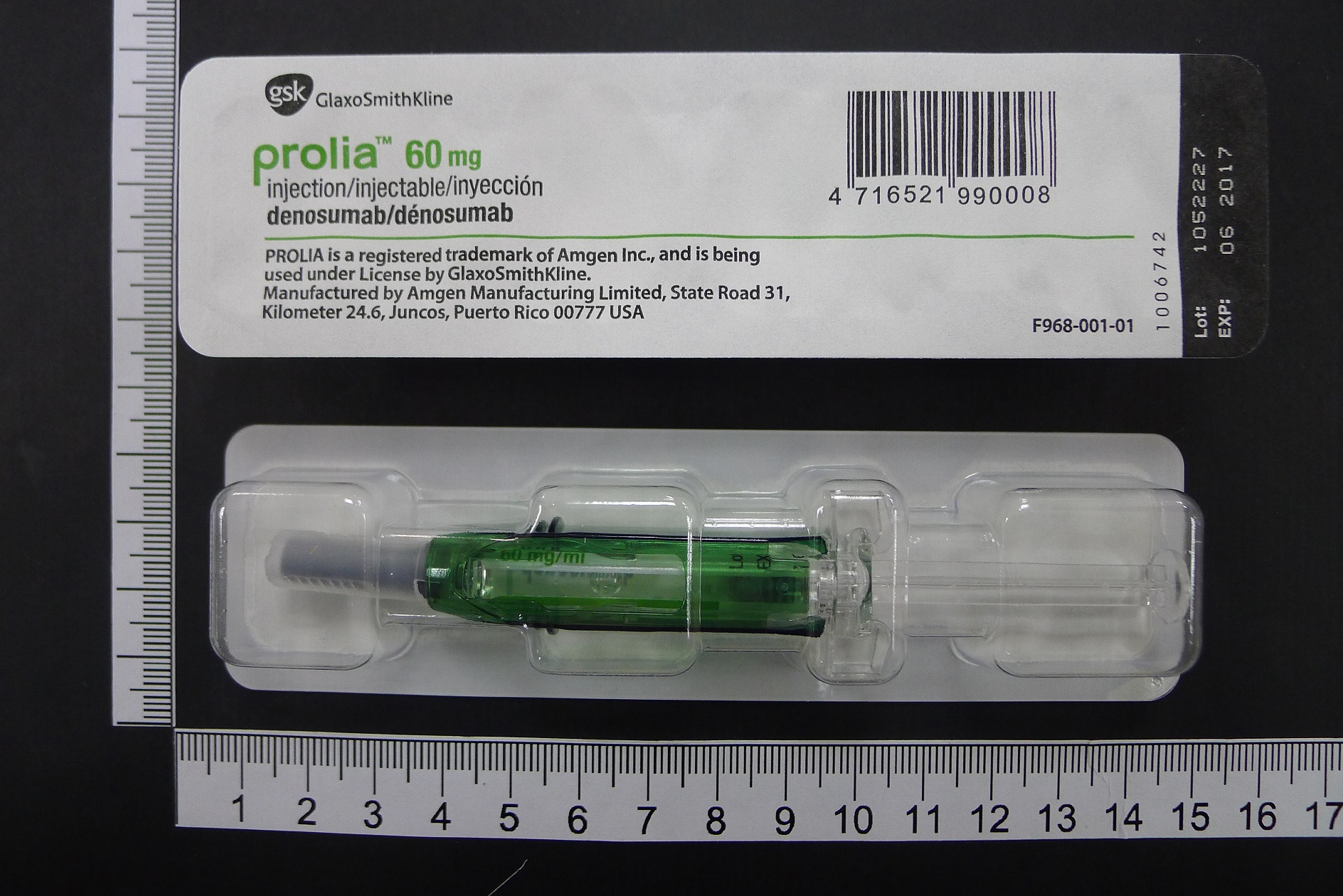
Prolia Inj -60mg |
|
保骼麗注射液 |
|
HE07P2 |
|
M05BX04 |
|
 JPG下載
JPG下載
|
|
DENOSUMAB |
|
60mg/1mL/Vial |
|
注射劑 |
|
Bone Resorption Inhibitors |
|
|
|
台灣安進藥品有限公司 |
|
|
|
KC00918209 |
|
衛署菌疫輸字第000918號 |
|
治療有骨折高風險性之停經後婦女骨質疏鬆症。說明:有骨折高風險性之停經後婦女骨質疏鬆症,包含下列任一狀況:有骨質疏鬆症骨折病史、具有多項骨折危險因子、先前接受其他骨質疏鬆症療法失敗或無法耐受其他骨質疏鬆症療法之病患。對患有骨質疏鬆症之停經後婦女,Prolia可降低脊椎、非脊椎和髖骨骨折的發生率。 治療有高度骨折風險之骨質疏鬆症男性患者,以增加骨量(bone mass)。說明:Prolia 適用於治療有高度骨折風險(定義為有骨質疏鬆症骨折病史,或具有多項骨折危險因子)之骨質疏鬆症男性患者,或先前曾接受其他骨質疏鬆症療法失敗或無法耐受其他骨質疏鬆症療法的患者,以增加骨量(bone mass)。 治療因為非轉移性攝護腺癌而進行雄性荷爾蒙抑制治療且具高度骨折風險之男性患者的骨質流失現象。 |
|
避免骨質的流失,因而增加骨骼骨質密度。 |
|
D |
|
(1) 成人:每6個月1次,每次60 mg,於上臂、大腿或腹部皮下注射。
(2) 兒童:安全性及有效性尚未確立。 |
|
噁心、腹瀉、關節痛、頭痛、低血鈣。 |
|
(1) 曾對本品過敏者,禁止使用。
(2) 低血鈣症。
(3) 懷孕婦女。
(4) Prolia®與Xgeva®具有相同之活性成分(denosumab),病人接受Prolia®治療不應再使用Xgeva®。 |
|
(1) 請冷藏儲存於2-8℃,避光儲存。
(2) 施打前,請同原包裝盒自然回溫15-30分鐘。
(3) 離開冷藏後,置於室溫(30°C以下)可存放14日。
(4) 僅供皮下注射使用,建議施打於上臂、大腿或腹部。
(5) 使用本品期間,若發現有嚴重骨、關節或肌肉疼痛,以及下顎骨關節壞死症狀(如:疼痛、腫脹、下顎或牙齦感染、麻木、牙齦流失等),請立即停藥,儘速就醫。
(6) 使用本品期間,建議每日補充至少1000 mg的鈣質與至少400 IU的維生素D。 |
|
冷藏(2- 8℃)儲存,避免陽光直接照射;如發生變質或過期,不可再使用。 |
|
5.6.1抗骨質再吸收劑 (anti- resorptive)
1.藥品種類
(3)Human monoclonal antibody for RANKL (RANKL單株抗體):denosumab(如Prolia)
2.使用規定
(1)限用於停經後婦女(alendronate、zoledronate、denosumab及risedronate 35mg亦可使用於男性,risedronate 150mg不可使用於男性)因骨質疏鬆症(須經DXA 檢測BMD之T score≦ -2.5SD)引起脊椎或髖部骨折,或因骨質疏少症(osteopenia)(經DXA檢測BMD之-2.5SD
(2)治療時,一次限用一項藥物,不得併用其他骨質疏鬆症治療藥物。
(3)使用雙磷酸鹽類藥物,須先檢測病患之血清creatinine濃度,符合該項藥物仿單之建議規定。 |
|
|
|
|