
相關聯結
|
藥品資訊
 |
 |
 |
| |
藥品資訊內容
| 語音自動播報
|
|
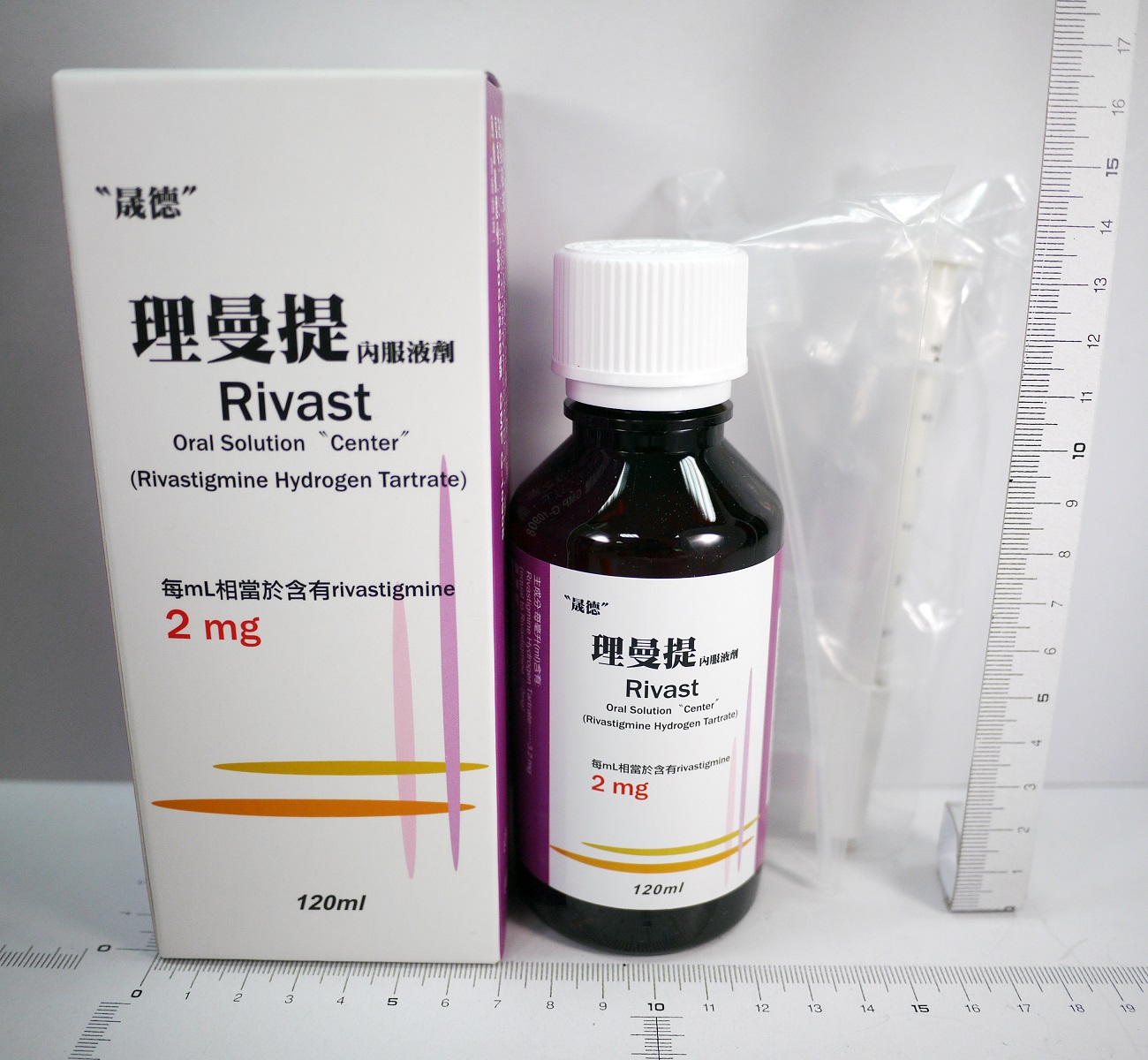
Rivast Oral Solution -2mg/ml |
|
理曼提內服液劑 |
|
BK09M1 |
|
N06DA03 |
|
 JPG下載
JPG下載
|
|
Rivastigmine Hydrogen Tartrate |
|
2mg/ml;120ml/Bot |
|
內服液劑 |
|
Parasympathomimetic agents |
|
|
|
晟德 |
|
|
|
AC52566157 |
|
衛署藥製字第052566號 |
|
輕度至中度阿滋海默型失智症。與帕金森氏相關的輕度至中度失智症。 |
|
Rivastigmine 藉由促進膽鹼的功能而產生療效,並藉由可逆性地抑制膽鹼酯酶的水解作用而增加乙醯膽鹼的濃度,可在極少數正常功能膽鹼神經元存在的情況下,減緩病程的發展。尚無證據顯示rivastigmine可改變潛在的失智症病程。 |
|
安全性尚未建立,因此懷孕婦女只有在治療利益大於對胎兒危險性下才能給藥。 |
|
●推薦起始劑量為1.5mg 一天兩次,可在早餐及晚餐後或一起服用,服用至少兩週後,若耐受性佳,可增加到3mg 一天兩次。再兩週後增加到4.5mg 一天兩次,再兩週後增加到6.0mg 一天兩次。任何劑量的增加都必須是在病患服用現有劑量至少已兩週且表現良好的耐受性情況下。
●如果在治療期間出現副作用(例如噁心、嘔吐、腹痛或食慾不振)或體重降低,則可能可以省略一個或更多的劑量,如果副作用持續,則劑量須降回先前有良好耐受性的劑量。
維持劑量
1.5mg到6mg 一天兩次,須保持在病患有良好耐受性的最高劑量。
每日最高劑量
6mg一天兩次。
中止後重新服用時的劑量
通常不良反應與發生率較常發生在高劑量時。如果病患中止服藥數天後,若重新服藥時,應從最低1.5mg 重新調整起,每隔兩週逐漸增加到有良好耐受性劑量。 |
|
可能會有噁心、嘔吐、腹瀉、食慾不振、腹痛、暈眩、頭痛、體重降低、躁動。 |
|
如果已知對於Rivastigmine 或處方中其他成分及其他Carbamate 衍生物有敏感性(hypersensitivity),則禁止使用Rivastigmine。
嚴重肝功能族群的研究尚未建立,故不可使用本品於該一族群之病人。 |
|
1. 請密封避光儲存於25℃以下,不須冷藏。
2. 嚴重肝功能不良者,不建議使用。
3. 服藥後如有噁心、嘔吐或厭食、體重減輕等症狀,請回診告知醫師。
4. 失智症可能會逐漸造成駕駛或操作機械能力的損害,請小心注意安全。 |
|
|
|
1.3.3.失智症治療藥品
1.限用於依NINDS-ADRDA或DSM或ICD標準診斷為阿滋海默氏症或帕金森氏症之失智症病患。
2.臨床診斷為「血管性失智症」,或有嚴重心臟傳導阻斷(heart block)之病患,不建議使用。(108/12/1)
3.初次使用者,需於病歷上記載以下資料:(106/10/1)
(1)CT、MRI或哈金斯氏量表(Hachinski lschemic Score)三項其中之任一結果報告。
(2)CBC, VDRL, BUN, Creatinine, GOT, GPT, T4, TSH檢驗。
(3)MMSE或CDR智能測驗報告。
4.依疾病別及嚴重度,另規定如下:
(1)阿滋海默氏症之失智症由神經科或精神科醫師處方使用。
Ⅰ.輕度至中度失智症:
限使用donepezil、rivastigmine及galantamine 口服製劑(90/10/1、92/1/1、95/6/1、100/3/1、102/8/1、106/10/1、108/5/1):
i.智能測驗結果為MMSE 10~26分或CDR 1級及2級之患者。
ii.使用前述三種藥品任一種後,三個月內,因副作用得換用本類另一種藥物,並於病歷上記載換藥理由。(93/4/1、102/8/1、106/10/1)
iii. 使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較前一次治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。 (98/1/1、99/5/1、102/8/1、106/10/1、108/5/1)
iv.使用rivastigmine貼片劑(如Exelon Patch),每日限用一片,且不得併用同成分之口服藥品(100/3/1)。
Ⅱ.中重度失智症:
限使用memantine口服製劑(95/6/1、99/10/1、102/8/1、106/10/1)
i. 智能測驗結果為10≦MMSE≦14分或CDR 2級之患者。
ii.曾使用過donepezil, rivastig-mine, galantamine其中任一種藥品之患者,若不再適用上述其中任一藥物,且MMSE或CDR智能測驗達標準(10≦MMSE≦14分或CDR 2級),得換用memantine。惟 memantine 不得與前項三種藥品併用。(106/10/1)
iii.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較前一次治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。惟Ebixa Tablets及Evy Tablets等2種藥品,使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(98/1/1、99/5/1、102/8/1、106/10/1)
Ⅲ.重度失智症:(99/10/1、102/8/1、108/5/1)
限使用donepezil及memantine口服製劑 (102/8/1、108/5/1)
i.智能測驗結果為MMSE 5-9分且CDR 3級之患者。
ii.臥床或無行動能力者不得使用。
iii.曾使用過memantine,donepezil, rivastigmine, galantamine而不再適用者,不得使用。
iv.donepezil及memantine二者不能併用。
v.使用後每一年需重新評估,追蹤MMSE智能測驗,如MMSE較前一次治療時減少2分(不含)以上,則應停用此類藥品。惟Ebixa Tablets 及Evy Tablets等2種藥品,使用後每一年需重新評估,追蹤MMSE智能測驗,如MMSE較起步治療時減少2分(不含)以上,則應停用此類藥品。(99/10/1、102/8/1、108/5/1)
(2)帕金森氏症之失智症(99/5/1、100/3/1、102/8/1)
限神經科醫師診斷及處方使用於輕度至中度之失智症。
限使用rivastigmine口服製劑 (102/8/1)
Ⅰ.智能測驗結果為MMSE 10~26分或CDR 1級及2級之患者。
Ⅱ.失智症發生於帕金森氏症診斷至少一年以後。
Ⅲ.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,如MMSE較前一次治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(99/5/1、102/8/1) |
|
|
|
|
|
|
 |
 |
 |
|