
相關聯結
|
藥品資訊
 |
 |
 |
| |
藥品資訊內容
| 語音自動播報
|
|
Ozurdex Inj -0.7mg |
|
傲迪適眼後段植入劑 |
|
AD05P2 |
|
S03BA01 |
|
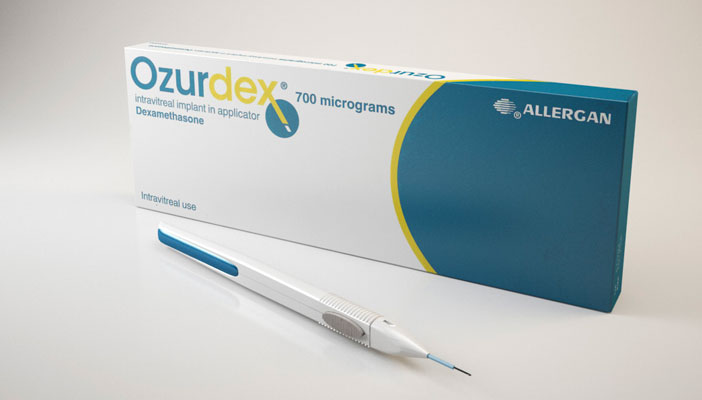 JPEG下載
JPEG下載
|
|
DEXAMETHASONE |
|
0.7mg/Vial |
|
注射劑 |
|
EENT - Corticosteroids |
|
|
|
台灣愛力根藥品股份有限公司 |
|
|
|
BC25360200 |
|
署藥輸字第025360號 |
|
因 BRVO (Branch Retinal Vein Occlusion) 或 CRVO (Central Retinal Vein Occlusion) 導致黃斑部水腫。用於影響眼後段的非感染性葡萄膜炎的治療。 糖尿病黃斑部水腫 (DME)所導致的視力損害。 |
|
Dexamethasone 是一種強效皮質類固醇,已被證實可控制發炎現象。 |
|
C |
|
建議劑量為罹病眼部玻璃體內注射一劑 OZURDEX®植入物。不建議雙眼同時接受注射。 |
|
使用皮質類固醇,包括dexamethasone 700µg 可能造成後囊下白內障(posterior subcaspsular cataracts)、眼內壓上升與青光眼,也可能因細菌、真菌或病毒造成繼發性眼部感染。 |
|
禁用於:
1. 對其活性成分或任一賦形劑過敏者。
2. 具有或疑似具有眼部或眼周感染(Periocular infection),包括大部分發生於角膜與結膜的病毒性疾病,例如活動性單純皰疹病毒性上皮角膜炎(樹枝狀角膜炎)、牛痘(vaccinia)、水痘、分枝桿菌感染及真菌疾病。
3. 無法單靠藥物有效控制的晚期青光眼。
4. 晶狀體後囊部破裂之無晶狀體患眼。
5. 晶狀體後囊部破裂以及植入前房人工水晶體之患眼。 |
|
1. 病人接受 OZURDEX®玻璃體內注射後可能會出現短暫的視力下降。在視力恢復前不應開車或操作機器。
2. OZURDEX®僅限單次使用。每個注射器只能用於治療一隻眼睛。
3. 接受本品施打後,如果眼睛變紅、畏光、疼痛、或者出現視力改變時,應立即尋求眼科醫師的醫療照護。 |
|
室溫(15-30℃)儲存,避免陽光直接照射;如發生變質或過期,不可再使用。 |
|
14.9.4.Dexamethasone intravitreal implant (如Ozurdex) (104/05/1、105/8/1、106/4/1、108/4/1、109/2/1、109/3/1)
1.限眼科專科醫師施行。(109/2/1)
2.須於第一次申請核准後5年內使用完畢。(109/2/1)
3.用於非感染性眼後房葡萄膜炎病人,需符合下列條件:
(1)限地區醫院以上層級(含)施行。(109/2/1)
(2)需排除因感染性引起之眼後房葡萄膜炎如肺結核、梅毒、弓漿蟲等之感染。
(3)矯正後視力介於0.05和0.5之間。
(4)需符合下列治療方式之一:
Ⅰ.葡萄膜炎之患者以口服類固醇控制病情,反應不良或仍有發炎與黃斑部水腫者,需輔以cyclosporin或其他全身性免疫抑制劑,經前述治療眼睛發炎仍無法控制者。
Ⅱ.無法口服全身性藥物(類固醇或cyclosporin)控制者:
i.懷孕或正在授乳的婦女。
ii.罹患活動性的感染症的病患。
iii.身上帶有人工關節者,罹患或先前曾罹患過嚴重的敗血症(sepsis)者。
iv.惡性腫瘤或具有癌症前兆(pre-malignancy)的病患。
v.免疫功能不全者(Immunodeficiency)。
vi.曾因其他疾病服用上述口服全身性藥物,有嚴重併發症或後遺症者。
(5)每眼限給付1支。
(6)給付後六個月內不得使用cyclosporin藥品。
(7)需事前審查,並檢附病歷摘要及符合下列條件之一之診斷依據。
Ⅰ.一個月內有效之OCT 顯示中央視網膜厚度(central retinal thickness, CRT)≧300μm。
Ⅱ.一個月內有效之FAG (fluorescein angiography)看到血管明顯滲漏現象或黃斑部囊狀水腫。
4.用於中央視網膜靜脈阻塞(CRVO)導致黃斑部水腫,需符合下列條件:(105/8/1、106/4/1、108/4/1、109/2/1、109/3/1)
(1) 限18歲以上患者。
(2) 中央視網膜厚度(central retinal thickness, CRT)≧300μm。
(3) 已產生中央窩下(subfoveal)結痂者不得申請使用。
(4) 須經事前審查核准後使用。
Ⅰ.第一次申請以2支為限,第一次申請時需檢附一個月內之病眼最佳矯正視力(介於0.05~0.5(含)之間)、眼底彩色照片、FAG (fluorescein angiography)、OCT (optical coherence tomography)及相關病歷紀錄資料。若患者腎功能不全(eGFR<45mL/min/1.73m2或serum creatinine≧1.5mg/dL),或具有藥物過敏史者需檢附相關資料,得檢附足以證明其罹患疾病之光學共軛斷層血管掃描儀(optical coherence tomography angiography, OCTA)檢查結果代替FAG資料。(108/4/1、109/2/1)
Ⅱ.經評估需續用者,再次申請時需檢附第一次申請資料及再次申請前一個月內有改善證明之相關資料,每眼給付以 4支為限 。(109/2/1)
Ⅲ.第一次申請治療後,患者治療成果不彰或對原申請藥物產生不良反應者,得申請更換給付新生血管抑制劑(限ranibizumab及aflibercept擇一申請),申請時需檢送第一次申請資料及再次申請前一個月內有黃斑水腫仍具臨床活性且中央視網膜厚度(central retinal thickness,CRT)≧ 300μm之相關資料。(109/3/1)
Ⅳ.每人每眼申請更換給付不同作用機轉藥物以一次為限,申請更換給付新生血管抑制劑(如aflibercept或ranibizumab)者,以4支為限。(109/3/1)
5.用於糖尿病引起黃斑部水腫 (diabetic macular edema, DME)之病變,需符合下列條件:(106/4/1、108/4/1、109/2/1、109/3/1)
(1)中央視網膜厚度(central retinal thickness, CRT)≧300μm。
(2)已產生中央窩下(subfoveal)結痂者不得申請使用。
(3)近三個月內之糖化血色素(HbA1c)數值低於10%,並於每次申請時檢附近三個月內之檢查結果。
(4)須經事前審查核准後使用。
Ⅰ.未曾申請給付新生血管抑制劑(anti-angiogenic agents)者,第一次申請以3支為限,第一次申請時需檢附一個月內之病眼最佳矯正視力(介於0.05~0.5(含)之間)、眼底彩色照片、FAG (fluorescein angiography)、OCT (optical coherence tomography)、及相關病歷紀錄資料。(109/2/1)
Ⅱ.經評估需續用者,再次申請時需檢附與第一次申請項目相同之各項最近檢查紀錄外,並檢送使用後有改善證明之相關資料,每眼給付以5支為限。(109/2/1)
Ⅲ.第一次申請治療後,患者治療成果不彰或對原申請藥物產生不良反應者,得申請更換給付新生血管抑制劑(限ranibizumab及aflibercept擇一申請),申請時需檢送第一次申請資料及再次申請前一個月內有黃斑水腫仍具臨床活性且中央視網膜厚度(central retinal thickness,CRT)≧ 300μm之相關資料。(109/3/1)
Ⅳ.每人每眼申請更換給付不同作用機轉藥物以一次為限,申請更換給付新生血管抑制劑者,以3支為限。(109/3/1)
(5)有下列情況不得申請使用:
Ⅰ.因其他因素(如玻璃體牽引)所造成之黃斑部水腫。(108/4/1)
Ⅱ.青光眼。 |
|
|
|
|
|
|
 |
 |
 |
|