
相關聯結
|
藥品資訊
 |
 |
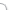 |
| |
藥品資訊內容
| 語音自動播報
|
|
Exelon Patch 5 |
|
憶思能穿皮貼片5 |
|
BK05E1 |
|
N06DA03 |
|
 JPG下載
JPG下載
|
|
RIVASTIGMINE |
|
9 mg/5 cm2, 4.6 mg/24 hr/pce |
|
貼片 |
|
Parasympathomimetic agents |
|
台灣諾華股份有限公司 |
|
|
|
B0252343FA |
|
衛署藥輸字第025234號 |
|
輕度至中度阿滋海默氏病之癡呆(失智)症。 |
|
1)本品是carbamate型態的中樞選擇性乙醯膽素酯酶抑制劑,因此被視為主動的膽素神經傳遞作用,可以減緩膽素神經元所分泌的乙醯膽素降解。
(2)從動物的研究數據證實,本品可以選擇性地增加大腦皮層及海馬中的乙醯膽素之利用率,因此本品可以改善乙醯膽素缺乏所導致的阿滋海默氏症。
(3)同時乙醯膽素酯酶抑制劑;可以減緩澱粉酶原的β-澱粉前驅物蛋白質片段(APP)的形成,澱粉嵌片是阿滋海默氏主要的病理學症狀之一。
穿皮貼片劑型,藉由穩定緩和的藥品傳輸方式,延長達最高血中濃度的時間、降低最高血中濃度、減低血中藥品濃度的波動幅度,達到減少腸胃道副作用產生,進而增進療效及順服性。且對於無法吞嚥,拒絕服藥,或是服用多種藥品的病人,可提供其方便的投與方式,降低照護者的照顧難度。 |
|
B |
|
1.初次使用:起始劑量為1天1片。
2.由口服劑型轉換為穿皮貼片劑型:
對於每日劑量小於6 mg之病人,若其耐受性良好且治療情況穩定達4週以上時,可轉換為Exelon Patch 5,1天1片,於最後1次服用口服藥物後的隔天開始使用貼片。
3.肝、腎功能不全病人無須調整劑量。
2.用法:
(1) 貼於清潔、乾淨、無毛髮、完整健康的皮膚上,不可貼在有塗抹乳膏、乳液或粉的皮膚上,最佳黏貼部位為上背或下背部,其次為上臂或胸部,貼片不可剪裁或摺疊。
(2) 每24小時更換新的貼片,應先撕下舊片再貼上新片,並且變換不同部位黏貼,以避免對皮膚產生刺激性,相同的部位於14天內不宜重複黏貼。
(3) 撕下舊片後,將黏貼的一面向內對摺壓緊後,放進原來的保護袋中,小心丟棄在兒童及動物不會觸及的地方。 |
|
1.常見為噁心、嘔吐、腹瀉、厭食、體重減輕等。
2.嚴重副作用如憂鬱、嚴重意識混亂、幻覺、腦中風、昏倒、心跳異常、胃潰瘍、腸胃道出血、錐體外症狀如顫抖等,請盡速就醫 |
|
已知對rivastigmine過敏,或對其他的carbamate衍生物(例如neostigmine、pyridostigmine、physostigmine)過敏者。 |
|
1.體重低於50公斤之病人可能發生較多的不良反應,且較可能因不良反應而停藥,在調整劑量時應特別小心。
2.膽鹼作用的增加可能造成以下情況,應特別注意:減緩心跳、在麻醉時會加強succinylcholine-type 肌肉鬆弛劑的作用、尿道阻塞、引發癲癇、使錐體外症狀惡化(如:顫抖)。氣喘或慢性肺阻塞疾病之病人使用時也應特別注意。
3.若因不當使用貼片造成過量時,應該立即撕下貼片,且在24小時內不可以再貼。在必要時,可以使用atropine治療,建議初始劑量為靜脈注射0.03 mg/kg atropine sulfate。 |
|
藥品應置於攝氏 15 ~ 25 度乾燥處所;如發生變質或過期,不可再食用。 |
|
1.3.3. 失智症治療藥品
1.限用於依NINDS-ADRDA或DSM或ICD標準診斷為阿滋海默氏症或帕金森氏症之失智症病患。
2.如有腦中風病史,臨床診斷為「血管性失智症」,或有嚴重心臟傳導阻斷 (heart block)之病患,不建議使用。
3.需經事前審查核准後使用,第一次申請須檢附以下資料:
(1) CT、MRI或哈金斯氏量表(Hachinski lschemic Score)三 項其中之任一結果報告。
(2) CBC, VDRL, BUN, Creatinine, GOT, GPT, T4, TSH檢驗。
(3)病歷摘要。
(4)MMSE或CDR智能測驗報告。
4.依疾病別及嚴重度,另規定如下:
(1)阿滋海默氏症之失智症
由神經科或精神科醫師處方使用。
Ⅰ.輕度至中度失智症:
限使用donepezil (如Aricept),rivastigmine (如Exelon) (90/10/1),galantamine (如Reminyl) (92/1/1、95/6/1、100/3/1):
i.智能測驗結果為MMSE 10~26分或CDR 1級及2級之患者。
ii.使用前述三種藥品任一種後,三個月內,因副作用得換用本類另一種藥物,不需另外送審,惟仍應於病歷上記載換藥理由。(93/4/1)
iii.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(98/1/1、99/5/1)
iv.使用 rivastigmine貼片劑 (如Exelon Patch),每日限用一片,且不得併用同成分之口服藥品(100/3/1)
Ⅱ.中重度失智症:
限使用memantine (如Witgen、Ebixa)(95/6/1、99/10/1)
i.智能測驗結果為10≦MMSE≦14分或CDR 2級之患者。
ii.曾使用過donepezil, rivastigmine, galantamine其中任一種藥品之患者,若不再適用上述其中任一藥物,且MMSE或CDR智能測驗達標準(10≦MMSE≦14分或CDR 2級),並經事前審查核准後得換用memantine。惟 memantine 不得與前項三種藥品併用。
iii使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(98/1/1、99/5/1)
Ⅲ.重度失智症:(99/10/1)
限使用donepezil (如Aricept)、memantine (如Witgen、Ebixa)
i.智能測驗結果為MMSE 5-9分且CDR 3級之患者。
ii.臥床或無行動能力者不得使用。
iii.曾使用過memantine,donepezil, rivastigmine, galantamine而不再適用者,不得使用。
iv.donepezil及memantine二者不能併用。
v. 使用後每一年需重新評估,追蹤MMSE智能測驗,如MMSE較起步治療時減少2分(不含)以上,則應停用此類藥品。
(2)帕金森氏症之失智症(99/5/1、100/3/1)
限神經科醫師診斷及處方使用於輕度至中度之失智症。
限使用rivastigmine口服製劑 (如Exelon Capsule)
Ⅰ.智能測驗結果為MMSE 10~26分或CDR 1級及2級之患者。
Ⅱ.失智症發生於帕金森氏症診斷至少一年以後。
Ⅲ.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(99/5/1)
備註:
起步治療定義:係指同組藥品第一次申請同意治療之評分 |
|
|
|
|
|
|
 |
 |
 |
|