藥品資訊內容
| 語音自動播報
|
|
Tarceva Tab-150mg |
|
得舒緩膜衣錠150毫克 |
|
KF09M1 |
|
L01EB02 |
|
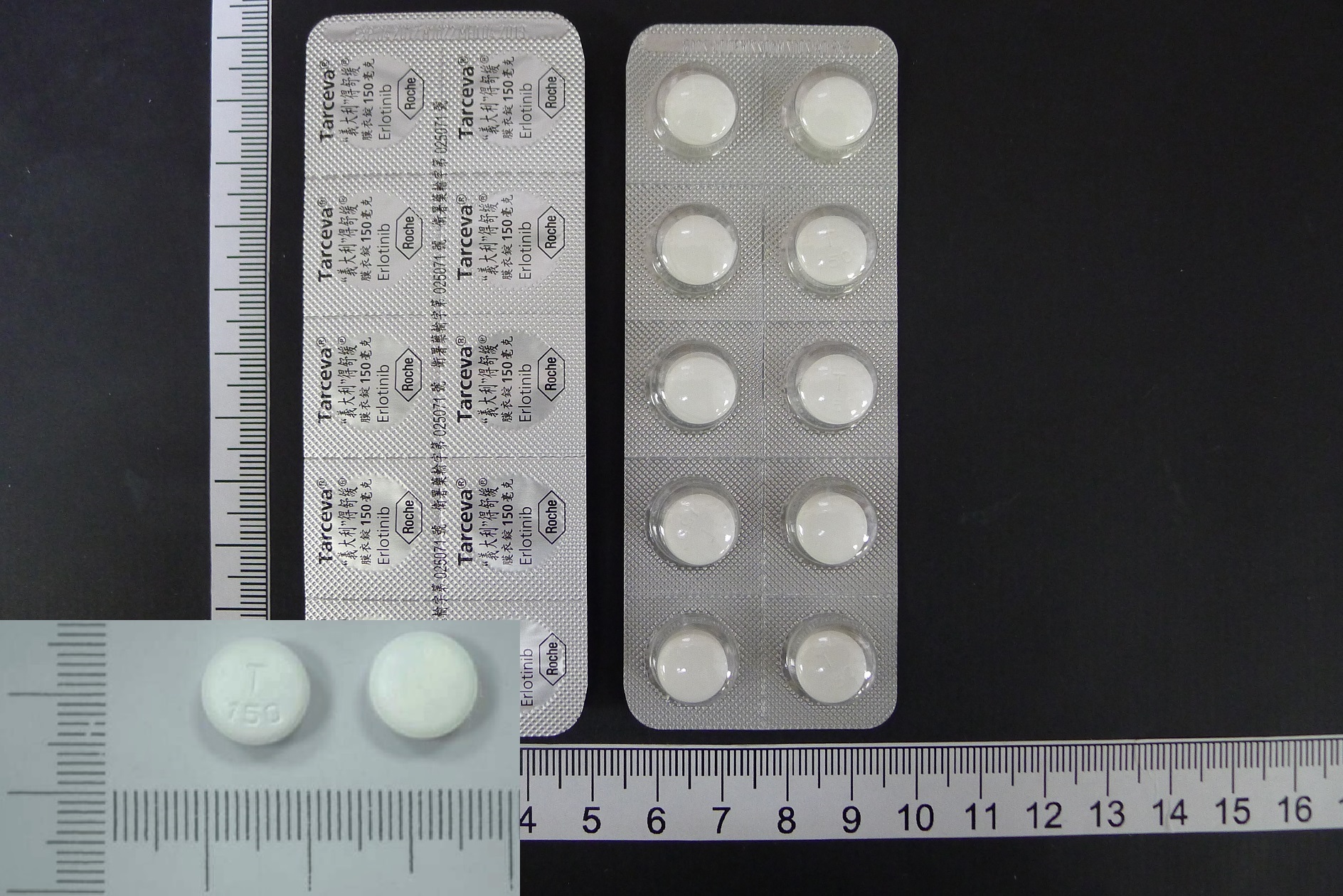 JPG下載
JPG下載
|
|
ERLOTINIB TAB-150mg |
|
150mg |
|
錠劑 |
|
Antineoplastic Agents |
|
羅氏大藥廠股份有限公司 |
|
|
|
B024407100 |
|
衛署藥輸字第024407號 |
|
適用於具有EGFR-TK突變之局部侵 犯性或轉移性之非小細胞肺癌(NSCLC)病患之第一線治療。適用於先前已接受過化學治療後,但仍局部惡化或轉移之肺腺癌病患之第二線用藥。適用於已接受 4個週期含platinum-based第一線化學療法且尚未惡化的局部晚期或轉移性肺腺癌的維持療法。 |
|
Erlotinib為quinazoline 衍生物,化學結構與gefitinib(IressaÒ)類似,可選擇性抑制EGFR-TK(epidermal growth factor receptor-tyrosine kinase)的活性,其結合在 tyrosine kinase的 ATP上, 使細胞的磷酸化作用 (phosphorylation) 受抑。由於癌細胞的 EGFR 過度表現,抑制此受體可抑制癌細胞增殖、分化、細胞存活及轉移。 |
|
D |
|
1.每天一次,每次150毫克,持續治療直至疾病惡化或發生無法忍受的毒性。
2.下述情況需作劑量調整(以50毫克作調降單位)或暫停給藥:
i.發生嚴重皮膚反應、無法以loperamide治療或是嚴重脫水的腹瀉。
ii.發生嚴重肝毒性(第3或第4級) |
|
1.常見:體重減輕、食慾不振、衰弱、噁心、嘔吐及腹部不適。
2.主要:紅疹、搔癢、腹瀉、肝指數上升、凝血時間延長、消化道出血、結膜角膜炎
3.嚴重:間質性肺炎與心肌梗塞。 |
|
1.對Erlotinib過敏者禁用。
2.對孕婦和哺乳期婦女尚無資料證明可安全應用。 |
|
1.使用於18歲以下兒童之安全性及有效性尚未建立,而老年人無須調整劑量。
2.本藥主要經由肝臟代謝及膽汁排泄,肝功能不全的患者須小心使用,若發生嚴重的副作用時,需考慮調降劑量或停藥 。
3.本藥可能發生嚴重且致命性的間質性肺炎,若病人發生急性新的肺部症狀或原有肺部症狀急性惡化(如呼吸困難、咳嗽及發燒等),需暫停使用本藥直到診斷確立。如果確診為間質性肺疾病,必須停用erlotinib,並給予適當的治療。
4.本藥懷孕用藥安全分級為 D,於動物試驗顯示會造成胚胎或胎兒死亡,因此女性必須在用藥期間及停藥後至少2週內採取避孕措施。
5.本藥是否分泌至乳汁未明, 不建議授乳。 |
|
藥品應置於攝氏 15 ~ 25 度乾燥處所;如發生變質或過期,不可再食用。 |
|
9.29.Erlotinib(如Tarceva):(96/6/1、96/8/1、97/6/1、101/5/1、101/10/1)
1.限單獨使用於
(1)先前已使用過第一線含鉑化學治療,或70歲(含)以上接受過第一線化學治療,但仍局部惡化或轉移之腺性非小細胞肺癌之第二線用藥。(97/6/1)
(2)先前已使用過platinum類及docetaxel或paclitaxel化學治療後,但仍局部惡化或轉移之非小細胞肺癌之第三線用藥。
2.需經事前審查核准後使用,若經事前審查核准,因臨床治療需轉換同成份不同含量品項,得經報備後依臨床狀況轉換使用,惟總使用期限不得超過該次申請事前審查之療程期限。(97/6/1)
(1)用於第二線用藥:檢具確實患有非小細胞肺癌之病理或細胞檢查報告,並附曾經接受第一線含鉑化學治療,或70歲(含)以上接受過第一線化學治療之證明,及目前又有疾病惡化之影像診斷證明(如胸部X光、電腦斷層或其他可作為評估的影像),此影像證明以可測量(measurable)的病灶為優先,如沒有可以測量的病灶,則可評估(evaluable)的病灶亦可採用。(97/6/1)
(2)用於第三線用藥:檢具確實患有非小細胞肺癌之病理或細胞檢查報告,並附曾經接受第一線及第二線化學藥物如platinum(cisplatin或carboplatin)與 taxanes(paclitaxel或docetaxel)治療之證明,及目前又有疾病惡化之影像診斷證明(如胸部X光、電腦斷層或其他可作為評估的影像), 此影像證明以可測量(measurable)的病灶為優先,如沒有可以測量的病灶,則可評估(evaluable)的病灶亦可採用。(97/6/1)
(3)每次申請事前審查之療程以三個月為限,每三個月需再次申請,再次申請時並需附上治療後相關臨床資料,如給藥四週後,需追蹤胸部X光或電腦斷層等影像檢查一遍,評估療效,往後每四週做胸部X光檢查,每隔八週需追蹤其作為評估藥效的影像(如胸部X光或電腦斷層)。(101/5/1)
3.醫師每次開藥以4週為限。
4.本藥品與gefitinib (如Iressa) 不得併用。 |
|
|
|
|