NEW!!!
2024.01.22公告:
文件相關表單於2024.01.22即日起實施使用新表單。
NEW!!!
經109/12/21會議決議,有關回溯性計畫:資料回溯期限最晚至送件前一個月。
轉知~~~
中華民國110年10月26日衛授食字第1101409136號公告,衛生福利部已修訂「藥品臨床試驗申請須知」,可至食品藥物管理署網站>業務專區>藥品>臨床試驗(含BE試驗)>臨床試驗相關法規)專區下載相關參考資料。
轉知~~~
衛生福利部中華民國110 年6 月25 日衛授食字第,衛生福利部已修訂「嚴重特殊傳染性肺炎防疫期間藥品臨床試驗執行之建議及原則」及「嚴重特殊傳染性肺炎防疫期間藥品臨床試驗執行之建議及原則問答說明事項」可至衛生福利部食品藥物管理署網站業務專區藥品>臨床試驗(含BE試驗)專區下載參考
---------------------------------------------------------
1.會議日期:
113年度:
113.01.15(一)、113.02.26(一)、113.03.18(一)、113.04.15(一)、113.05.20(一)、113.06.17(一)、113.07.15(一)、113.08.19(一)、113.09.23(一)、113.10.21(一)、113.11.18(一)、113.12.16(一)
送審資料需於召開會議前二週完成審查,始得入會審查
2.聯絡方式:
●人體試驗委員會承辦人:林慧卿組長、林炳璇管理師、張毓芸管理師
●電話:(02)2219-3391分機66004、專線:(02)2219-0651
●E-mail:irb.cth@gmail.com
●地址:新北市新店區中正路362號A棟8樓821室 人體試驗委員會
3.計畫試驗經費及合約事宜:
請洽醫學研究中心 (02)2219-3391 分機66008
E-mail: clinicaltrial.cth@gmail.com
4.衛生福利部認證:
本委員會通過衛生福利部人體研究倫理審查委員會查核作業,合格有效期間自113年1月1日至118年12月31日止
5.【公告】:
函轉台灣受試者保護協會有關CITI Program使用方式相關事宜,詳見附件
6.【衛生署公告】:
行政院衛生署於101.07.05衛生署公布實施「得簡易程序審查之人體研究案件範圍」、「得免研究對象同意之人體研究案件範圍」及「得免IRB審查之人體研究案件範圍」
7.【公告】:
行政院衛生署於100.06.09重申,醫療機構施行人體試驗,應確實遵守人體試驗管理辦法第11條規定「不得向受試者收取人體試驗有關之任何費用」,亦不得申請健保支付,詳見附件
8.受理受試者申訴:
電話:(02)2219-3391分機66004。專線:(02)2219-0651。
E-mail:irb.cth@gmail.com |
*********************************************************
自公告日起,廠商委託執行之人體試驗收費標準如下: (2015年08月24日起簽訂之合約適用)
1.新案審查費:伍萬元。
2.CIRB、NRPB、JIRB追認新案審查費:陸萬元。
3.管理費:參萬元;如涉及藥品試驗加收藥品管理費第一年參萬伍仟元,次年以上,每年收貳萬元。
4.有關廠商委託之臨床試驗,本院之臨床試驗案於108年9月1日起調漲其收費,其病人接受試驗之門診、住院、急診其醫療費用(含檢驗、檢查)皆以1.5倍自費價計算。
有關已簽訂合約之臨床試驗案,待臨床試驗修訂合約書簽立後實施。 |
**********************************************************
個案報告審查相關規定(108/08/01公告):
1.本標準作業程序適用於欲公開發表之臨床個案報告。
2.申請流程請詳見標準作業程序IRB042。
3.本會於108/09/01起審查個案報告,表單請自"相關表單"下載。
**********************************************************
自107年02月12日起,經委員會會議決議,為保護本院臨床試驗受試者,計畫主持人應為本院專任受聘之醫師,以保障受試者權利、安全及福祉。
**********************************************************
依2021.10.18會議決議,即日起至疫情狀況趨緩降級前線上課程與實體課程時數不要求比例。可認列【臺灣學術倫理教育資源中心】、【台灣臨床試驗教育訓練中心】教育訓練時數,但【臺灣學術倫理教育資源中心】課程僅認列其IRB/REC類別課程時數。 |
|
|
|
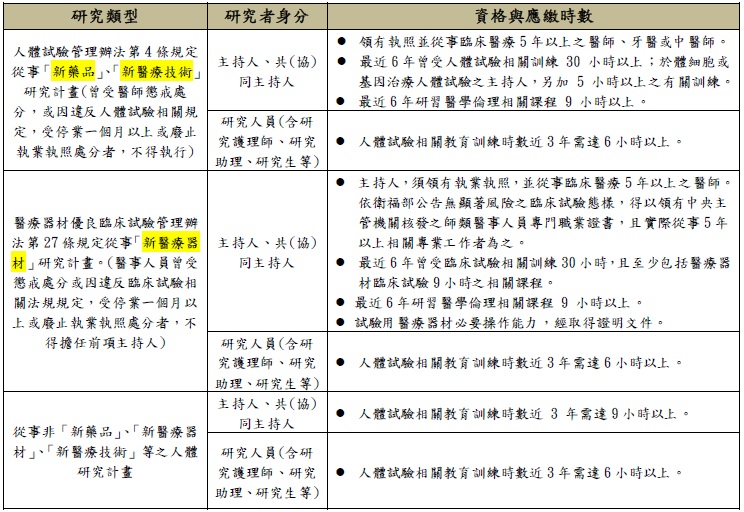 研究團隊成員教育訓練時數規範(2021.12.20會議修訂)
研究團隊成員教育訓練時數規範(2021.12.20會議修訂) |
|
|
|
|